Schlagwort: ‘Drug Saftey’
Flight inspection – GSP certificates of five pharmaceutical enterprises were withdrawn
Since August, Hunan Food and Drug Administration has started specific rectifications in the field of drug distribution. Hundreds of drug manufacturers and operating enterprises had the flight inspections. Problems were found in five pharmaceutical enterprises during the flight inspections. Their GSP certificates were withdrawn. (Source: Sanxiang City Express)
药品“飞检” 5家药企被约谈撤证
来源:三湘都市报 2016-08-25
核心提示:从八月开始,湖南省食药监局开展药品流通领域专项整治,数百家药品生产经营企业接受飞行检查,已有5家药企在“突袭”中露出马脚,被撤GSP(药品经营质量管理规范)证书。
[hide for= “!logged”]
不打招呼、不用陪同和接待,直奔现场,发现问题立即查处……近期,湖南药企老总们的“朋友圈”屡屡被这些内容刷屏。从本月开始,我省食药监局开展药 品流通领域专项整治,数百家药品生产经营企业将接受飞行检查,已有5家药企在“突袭”中露出马脚,被撤GSP(药品经营质量管理规范)证书。
曝光药企5类违规行为
8 月22日,因为飞行检查中发现违规行为,湖南长发丰源医药有限公司、湘潭恒健医药有限责任公司、娄底市华泰医药有限公司、岳阳康尔医药有限公司、益阳三和 药业有限公司5家药品批发企业的“老总”被省食药监局约谈。五家企业因此受到撤GSP(药品经营质量管理规范)证书的处罚,在行业内引发关注。
这 将是药品流通领域史上最严的一次专项整治行动。省食品药品监管局药品流通处相关负责人表示,药品飞行检查是药品监督管理部门针对药品生产经营等环节开展的 不预先告知的突击检查或者暗访调查。从当日公布的首批飞行检查情况来看,目前,湖南整体上药品流通企业比较规范,但也有个别企业存在违规行为。主要存在五 大方面的问题:仓库温湿度控制系统运作不规范,中药饮片违规分包装,未在核准经营场所范围进行经营活动,零售连锁企业未完全实行统一配送,个别财务转账出 现公对私的情形。
“飞检”将成监管常规动作
省食药监局介绍,选择飞行检查对象并非漫无目 的,而是耙向挑选。那些药品市场抽检不合格、药品出现严重或聚集性不良反应、既往诚信状况差以及被投诉举报的企业是“飞检”的主要目标。为使每一次飞行检 查出其不意,将推出严格的保密措施。飞行检查前,被检企业所有信息严格保密,连检查小组组长都无从获知。抵达目的地后,需在全体组员的共同见证下开启信 封,才知道被检企业。
据悉,执法检查部门接下来将依托飞行检查这一重要载体,在检查对象上,重点针对农村、乡镇、边远零售药店和企业诚信等次较低、日常监管存在问题较多的药店。
影响
“药品飞行检查”将加速行业洗牌
实 际上,国家食药监总局早在2006年就发布了《关于印发药品GMP飞行检查暂行规定的通知》,但直至去年11月和今年初才进一步出台了《药品飞行检查办法 (征求意见稿)》和《药品飞行检查办法(草案)》。湖南多位药品流通领域的负责人告诉记者,“以前飞检是国家食药监总局在管,地方并未响应。自国家发布四 个最严以来,药品监管逐渐强化,特别是今年开始,湖南省也相应开展了飞检活动。”
逐渐加大力度的飞检将加速药品行业洗牌。一位药品连锁机构 的负责人表示,中小制药和流通企业一旦正规操作,利润就会大打折扣,有些甚至会亏本,因此就有了简化生产流程、篡改生产工艺等不合规行为。他认为,“常态 化的飞检肯定让不少药企在严查中暴露问题,届时,或将迎来药企的停产大潮。”
[/hide]
Zhejiang Pharma got warning from FDA, which might affect the market exploitation in the US
On 11th August, Zhejiang Pharma, which is the biggest Vitamin E manufacturer, announced that the subordinate company – Xinchang Pharmaceutical factory – got a warning letter from U.S. Food and Drug Administration. From the on-site inspection, FDA found three defects which did not meet the requirements of cGMP. The factory is ordered to make rectifications. Many experts from the industry worry that the warning might affect its market exploitation in the US. (Source: Pharmnet)
浙江医药子公司遭FDA警告 恐波及美国市场开拓
来源:医药网 2016-08-22
核心提示:8月11日,国内维生素E产量最大的浙江医药股份有限公司发公告称,公司下属企业新昌制药厂收到美国食品药品监督管理局发出的警告信。FDA现场检查发现,新昌制药厂处置不符合cGMP规定的三条缺陷,并责令整改。浙江医药正根据要求整改。多位业内人士担忧,浙江医药子公司遭FDA警告恐波及其美国市场的开拓。
[hide for= “!logged”]
国内维生素E产量最大的浙江医药股份有限公司(以下简称“浙江医药”,600216.SH)连发两则公告称,公司下属企业新昌制药厂收到美国食品药品监督管理局(以下简称“FDA”)发出的警告信,正根据要求整改。
8月11日,浙江医药公告称,FDA现场检查发现,新昌制药厂处置不符合cGMP规定的三条缺陷,并责令整改。不过,浙江医药尚未披露整改进展,FDA也未作出相关产品能否进入美国市场的进一步措施。
而今年3月,浙江医药刚与浙江华海药业股份有限公司全资子公司华海(美国)国际有限公司签署《战略合作框架协议》,双方合作的重点是原料药及制剂产品在美国市场的业务合作。
多位业内人士担忧,浙江医药子公司遭FDA警告恐波及其美国市场的开拓。针对上述问题,《中国经营报》记者致电、致函浙江医药,截至发稿未获回复。
FDA警告
浙江医药是国内重要的维生素生产厂家,目前已经形成了脂溶性维生素、类维生素、喹诺酮类抗生素、抗耐药抗生素等系列产品的专业化、规模化生产,其中原料产品维生素E、天然维生素E产量、β-胡萝卜素和斑蝥黄素等产量均居国内首位。
8月10日、11日,浙江医药连续发布两则公告称,公司下属企业新昌制药厂于2016年8月10日收到FDA发出的警告信。
该 警告信是针对2015年6月15日至18日FDA在新昌制药厂的原料药现场检查,并指出了不符合cGMP的三条缺陷:实验室控制记录没有包括所有根据已有 规程和标准执行的符合性检测的完整数据;在电脑系统的权限控制或数据更改方面没有足够的控制措施,也没有对数据的缺失提供足够的预防控制措施;记录的及时 性。
FDA要求新昌制药厂作出整改并在15个工作日内回复。浙江医药表示,该警告信目前对公司生产、经营没有造成实质性影响,新昌制药厂将抓紧整改,并及时作出回复。
数 据显示,涉及新昌制药厂出口到美国的两个原料药2015年美国市场销售收入6026.1万元,占公司2015年营业收入比例为1.3%,毛利2821.4 万元,占公司2015年毛利比例为3.7%;2016年一季度销售收入2200.7万元,占公司2016年一季度营业收入比例为1.7%,毛利 1180.9万元,占公司2016年一季度毛利比例为4.6%。
FDA警告发出后,公司需对FDA的警告信作及时反馈,制定详细的纠正行动 计划,尽快查清数据完整性疏漏根源,采取临时措施来确保药品质量。中投顾问研究总监郭凡礼分析称,“从长远来看,公司需从程序、工艺、方法、控制、监管和 人力资源等多个方面进行补救或改善,以提高数据完整性及准确性。”
或影响美国市场开拓
早前,浙江医药就在为开拓海外市场积极奔走,美国市场一直是重点。而此次子公司遭到FDA警告,或影响公司相关产品在美国的市场开拓。
3月,浙江医药公告称,公司与浙江华海药业股份有限公司全资子公司华海(美国)国际有限公司于2016年3月7日签署了《战略合作框架协议》,合作的重点是原料药及制剂产品在美国市场的业务合作。
公告称,此次合作的目的在于充分发挥协议双方各自在药品生产、销售、研发、注册及国际认证等方面的优势,共同开发国际市场,促使企业转型升级,提升双方在国际医药市场的竞争力。
浙江医药表示,此次战略框架协议的签署,促使合作双方在优势互补、互惠互利、共同发展的基础上建立双赢的战略合作伙伴关系,进一步整合双方资源,共同进军美国医药市场。
本次收到FDA发出的警告信,是否将对浙江医药进军美国市场形成阻力?
郭 凡礼认为,想要进入美国市场,获得FDA认可是必不可少的敲门砖,也是证明企业产品质量、树立品牌形象的有效方式。“此次警告目前虽然未对公司生产经营造 成实质性影响,但后期整改不及时或是处理不当,将严重影响公司形象,产品也将无法取得FDA认证,国际市场竞争力会大大减弱,直接影响公司经营业绩。”
目前,浙江医药尚未披露整改进展,FDA也尚未作出相关产品能否进入美国市场的进一步措施,由此带来的进一步影响尚不得而知。
[/hide]
The storm of manufacturing technique inspections – manufacturers face crisis of production halts
CFDA made a draft about the announcement of carrying out the verification work of drug manufacturing technique. Since 11th August comments are solicited from the society until 10th September. The announcement says that every pharmaceutical manufacturer should carry out self-inspections of the manufacturing technique of every drug on the market. The content of the self-inspection is to check the accordance between the actual manufacturing techniques and the manufacturing techniques approved by the supervision departments. Besides, from 1st November 2016, CFDA will carry out flight inspections for drug manufacturers. (Source: 21st Century Business Herald)
生产工艺核查风暴来袭 药企面临停产危机
来源:21世纪经济报道 2016-08-12
核心提示:CFDA组织起草了《关于开展药品生产工艺核对工作的公告(征求意见稿)》,11日正式面向社会公开征求意见,征求时间截止到2016年9月10日前。该文件要求,各药企应对每个批准上市药品的生产工艺开展自查,自查内容为药品实际生产工艺与监管部门核准的生产工艺是否一致。此外,2016年11月1日起,国家食品药品监督管理总局将组织专家对药品生产企业开展飞行检查。
[hide for= “!logged”]
“大洗牌啊!”、“准备卸甲归田了”,8月11日晚间,某医药研发微信群里炸开了锅。
引起群成员集体恐慌的是药企生产工艺核查传言成真。CFDA组织起草了《关于开展药品生产工艺核对工作的公告(征求意见稿)》,11日正式面向社会公开征求意见,征求时间截止到2016年9月10日前。
这意味着,目前已经上市的药品,不论是中药、化药还是生物药,口服药还是制剂,国产药、原研药还是进口药,都必须进行生产工艺自查,并接受CFDA飞检。
生产工艺自查,不一致必须停产
据悉,为加强药品生产工艺管理,原国家食品药品监督管理局于2007年8月部署开展了注射剂类药品生产工艺和处方核查工作,各省局对企业申报登记的 生产工艺等相关资料进行了审查,初步建立了注射剂生产工艺等资料档案。2007年10月修订实施的《药品注册管理办法》规定批准药品上市前应进行生产现场 检查,保障了技术审评部门核定的生产工艺的可行性。
不过,“近年来,食品药品监管部门在监督检查中发现,仍有部分2007年前批准上市的品种未按照批准的生产工艺组织生产、改变生产工艺不按规定研究和申报。”
为此,该文件要求,各药企应对每个批准上市药品的生产工艺开展自查,自查内容为药品实际生产工艺与监管部门核准的生产工艺是否一致。
如果一致,则可以继续生产或进口,并到当地省级药监部门备案。“药品生产企业应于2016年10月1日前完成自查并将自查情况报所在地省级食品药品监管部门。省级食品药品监管部门应对企业自查情况进行汇总,于2016年11月1日前上报食品药品监管总局。”
如果不一致,相关药品生产企业应按照相关文件要求开展充分的研究验证。“经研究验证,生产工艺变化对药品质量产生影响的,企业应立即停产。”
与此同时,药品生产企业应于2017年6月30日前完成在产品种生产工艺的研究验证、提交补充申请等相关工作,其他暂不生产品种应于2017年12月31日前完成上述工作,“未按时完成的,应停止生产。”
飞检来袭,行业洗牌加剧
“之前的一致性评价好多企业都躲不过,但是它是针对化药的,这个是针对所有所有药品的,影响更大,”康臣药业药品研发中心研发副总经理郑兆广告诉记者,“国内药企应该存在很多生产工艺与注册工艺不一致的品种,这个跟中国制药行业的发展阶段有关。”
“自查之后的总局飞检也让药企很紧张,飞检力度应该很大,”另一名制药行业从业者则向记者透露:“这个文件对中小药企的影响更大,因为按照文件要求 正规操作,利润空间几乎就没有了,得倒闭。不按照文件的要求生产,也会被要求停产。因为接下来还要飞检,大药企也要重新审查,这个成本也是不小的,所以行 业即将迎来大洗牌。”
据了解,2016年11月1日起,国家食品药品监督管理总局将组织专家对药品生产企业开展飞行检查。检查中发现实际生产工艺与食品药品监管部门批准的生产工艺不一致的,依据《中华人民共和国药品管理法》第四十八条第二款的有关规定,其所生产的药品按假药论处。
而药监部门将依据《中华人民共和国药品管理法》第七十四条的有关规定对涉事药品生产企业进行处罚,并向社会公开相关企业法定代表人和相关责任人员。
[/hide]
Expired drugs can be recycled online
Recently, a public benefit activity to recycle expired drugs was held in Beijing. Except recycling household expired drugs in more than 200 cities nationally offline, household expired drugs can also be recycled online through many pharmaceutical e-commerce platforms, such as Ali Health. (Source: Health News)
网上也能回收过期药品
来源:健康报 2016-08-16
核心提示:近日,家庭过期药品回收公益活动在京启动。此次活动除了继续在全国200多个城市进行线下家庭过期药品回收外,还通过阿里健康等多家医药电商平台,开展网上家庭过期药品回收。
[hide for= “!logged”]
近日,家庭过期药品回收公益活动在京启动。此次活动除了继续在全国200多个城市进行线下家庭过期药品回收外,还通过阿里健康等多家医药电商平台,开展网上家庭过期药品回收。
活动期间,消费者可以通过天猫App扫描药品盒上的药监码,进入活动页面,了解药品是否过期等信息;之后点击页面最下方的链接跳转进入天猫广药白云山官方 旗舰店,进行登记注册,把家中符合回收细则条件的过期药品邮寄到指定地点;审核通过后,账号可获得代金券或满减券,在广药白云山官方旗舰店购买药品。除扫 码换药外,消费者也可以直接登录康爱多、好药师、广药健民网的天猫旗舰店广药白云山兑换专区参与活动。
[/hide]
Qingdao Center Hospital starts the first drug cold chain management in the province
Recently, Qingdao Center Hospital installed automatic temperature control devices to the cold storage facilities and the dispensing area in the drug buying office, Pharmacy Intravenous Admixture Services (PIVAS) and pharmacy department. If there are any abnormities, a text message will alarm the person in charge, so that it becomes possible to monitor the actual temperature of drugs and give an alarm. Thus, this hospital becomes the first one in Shandong to implement the whole cold chain drug management. (Source: Qingdao Evening News)
青岛市中心医院启动全省首个药品冷链管理模式
来源:青岛晚报 2016-07-13
核心提示:目前,青岛市中心医院分别在药品采购办、静配中心、药剂科等所有冷藏设备和调剂区安装自动温控装置。如果有异常直接发短信到负责人手机报警,实现了所有有关药品温度的实时监测和报警。这样,该院在岛城率先实施了药品的全程冷链管理。
[hide for= “!logged”]
高温天气让很多需要到医院取冷链药物的病人很头疼。如果长时间脱离冷链管理,药物很有可能将作废。为了缓解这种状况,近日,青岛市中心医院启动药品冷链管理全程无缝覆盖模式,消除原本冷链中药品从药房到科室和从门诊到家庭的两大“空窗期”,最大限度地保障患者用药安全。
全省首个启动全程无缝冷链
记者采访了解到,目前药品在生产环节、物流环节都有国家标准,各种制度规范比较齐全,但医院作为药品使用的终端环节,传统的药品配送采取开放式配送模 式,而冷链药品的院内冷链配送存在“断链”情况。“目前药品的冷链管理没有国家标准,从药房到科室,国家是允许存在30分钟的空窗时间的,但是患者用药还 是存在不安全因素。尤其我们医院以肿瘤为特色,很多肿瘤药品如高值靶向制剂、单克隆抗体等价格较高,管理上更应该加强,所以我们率先启动了全程冷链管 理。”市中心医院药剂科副主任孟向尚说。
中心医院院长兰克涛也告诉记者,医院想要实现全院的冷链管控投入成本相当巨大,大部分医院还处于观望状态,此前整个山东省还没有一家医院做到全程无缝 规范的冷链管理。之所以全面启动药品冷链管理系统,更多的是发挥公立医院的公益性,承担起更多的社会责任,保证患者的用药安全,特别是让肿瘤患者享受到与 国际接轨的用药服务。
冷链药品告别两大“空窗期”
据孟向尚介绍,很大一部分需要冷链管理的药物,如生物制剂、肿瘤化疗药品、血液制品、胰岛素系列等,需要的储存温度是2℃到8℃。但是目前,一个是药 品从病房配送到科室,另一个是病人把药品从门诊带回家,冷链药品存在着两大“空窗期”。“经常有病人来咨询,把药品放在太阳下晒了半天怎么办,我们一般都 是不建议使用。”孟向尚说。
目前,市中心医院分别在药品采购办、静配中心、药剂科等所有冷藏设备和调剂区安装自动温控装置,如果有异常直接发短信到负责人手机报警,实现了所有有 关药品温度的实时监测和报警。在门诊药房建设了岛城第一家药品阴凉区,购进了5台符合GSP标准的药品阴凉柜用来储藏温度要求在20℃以下的药物,在药品 采购办建设了容积达20立方米的冷藏库,在门诊窗口配备了1200多个保温袋和冰袋,并印制了冷链管理温馨提示卡,开展门诊患者的药品冷链管理和宣传。这 样,该院在岛城率先实施了药品的全程冷链管理,解决了院内的冷链药品配送和门诊患者的药品冷链管理。
200多种药品的使用者受益
“根据目前的医院药品目录,需要冷链管理的药品大约占到六分之一,有两百多种。我们配备的1000多个保温袋和冰袋,是根据我们药房近两个月来取药的 病人的人数测算出来的,病人来取药时,我们就会送上保温袋、冰袋和温馨提示卡,理论上一个月可以循环用一次,保温袋是免费给患者使用的,请大家一定要爱 惜,循环利用起来。”孟向尚说。
作为肿瘤特色医院,市中心医院还与医保特供药品定点药店合作,在日间肿瘤诊疗中心成立了青岛市首家肿瘤特殊药品注射中心,购置了两台带有自动记录功能的新型冷藏箱,以满足特殊储存条件药品的储存,实现了肿瘤药品的全程无缝管控,解决了肿瘤患者药品储存的后顾之忧。
“现在有26种医保特供药,这些药品很多单支价格很高,能达到几千元甚至上万元,如果患者希望自己的药物得到全程冷链管理,可以到药店进行说明,然后 直接到市中心医院日间肿瘤诊疗中心去使用就可以。”孟向尚说。记者在采访中也了解到,目前岛城还有几家医院也有药品冷链管理全程无缝隙覆盖的计划,已经启 动培训。
[/hide]
Four key contents are revised in the new GSP
On 20th July, CFDA announced the revise decision of the good supply practice (GSP). Since GSP was implemented on 1st June 2013, it has been revised twice on 1st July 2015 and 20th July 2016, respectively. The revise of GSP this time can be concluded as follows: 1. the documents which need to be checked from the first supplier are changed; 2. “requirements for the vaccination operation enterprises” is changed to “requirements for the vaccination delivery enterprises”; 3. Electronic supervision system is changed to drug tracing system; 4. The cold chain management shall be strengthened. (Source: Medicine Economic News)
新GSP四项关键内容调整
来源:医药经济报 2016-07-21
核心提示:2016年7月20日,CFDA出台新法规文件《国家食品药品监督管理总局关于修改〈药品经营质量管理规范〉的决定》。自原卫生部2013年6月1日施行的《药品经营质量管理规范》开始,至今共修订两次。第一次为2015年7月1日,第二次即为本次2016年7月20日。《药品经营质量管理规范》(GSP)内容具体变化,总结如下几点:1首营企业需要查验的证件资料收集变动;2“疫苗经营企业相关要求”调整为“疫苗配送企业要求”;3电子监管系统调整为药品追溯体系;4强化冷链管理。
[hide for= “!logged”]
2016年7月20日,CFDA出台新法规文件《国家食品药品监督管理总局关于修改〈药品经营质量管理规范〉的决定》(国家食品药品监督管理总局令第28号)。
回顾新版《药品经营质量管理规范》的修订历程,自原卫生部2013年6月1日施行的《药品经营质量管理规范》(中华人民共和国卫生部令第90号)开始,至今 共修订两次。第一次为2015年7月1日,CFDA发布的《药品经营质量管理规范》(国家食品药品监督管理总局令第13号),第二次即为本次总局第28号 令。
那么,经过两次修订,《药品经营质量管理规范》(GSP)内容具体发生了什么变化?根据笔者理解,总结如下几点:
1首营企业资料收集变动
在2015年7月1日的第一次《药品经营质量管理规范》(GSP)修订中,调整主要内容便是首营企业资料收集要求,将“营业执照年检证明”替换为“上一年度企业年度报告公示情况”,适应工商部门调整营业执照年度报告制度。
该 资料要求调整后,药品经营企业需修订企业质量管理体系文件,相应调整首营企业资料收集要求,并及时收集该项资料审核归档。另外,根据《国务院办公厅关于加 快推进“三证合一”登记制度改革的意见》(国办发[2015]50号),首营企业资料收集中,调整为“营业执照、税务登记、组织机构代码证复印件”。
2“疫苗经营企业相关要求”调整为“疫苗配送企业要求”
2016 年3月,由于发生疫苗事件,疫苗质量管理引起国家各执政部门高度重视,国务院于2016年4月份修订了《疫苗流通和预防接种管理条例》(中华人民共和国国 务院令第668号),规定疫苗生产企业直接向县级疾病预防控制机构配送第二类疫苗,或者委托具备冷链储存、运输条件的企业配送,减少疫苗多次经营流转,降 低由于运输、贮存温湿度监控不当所造成的对疫苗质变的风险。
本次新修订《药品经营质量管理规范》(GSP)中,适应国务院新管理条例的内容,严格监管疫苗质量管理,具备疫苗经营范围且受疫苗生产企业委托配送的经营企业,仍需严格按照新修订《药品经营质量管理规范》(GSP)第二十二条规定配置相应人员。
3电子监管系统调整为药品追溯体系
2016 年2月20日,CFDA发布《总局关于暂停执行2015年1号公告药品电子监管有关规定的公告》(2016年第40号),暂停了药品生产经营企业国家电子 监管相关工作。暂停期间,多个药品经营企业人员也曾咨询笔者,是否还需继续执行国家电子监管码“见码扫,数据上传”工作?是否真的完全取消电子监管码,那 么取消之后如何实现药品追溯性?
本次新修订《药品经营质量管理规范》(GSP),调整幅度最大的内容便是国家电子监管相关规定,调整后法规 中提出新字眼“药品追溯”,对药品流通环节中药品经营企业如何执行药品追溯制度提出操作性要求,新修订《药品经营质量管理规范》(GSP)中,明确“企业 应当在药品采购、储存、销售、运输等环节采取有效的质量控制措施,确保药品质量,并按照国家有关要求建立药品追溯系统,实现药品可追溯”“企业应当建立能 够符合经营全过程管理及质量控制要求的计算机系统,实现药品可追溯。”
4强化冷链管理
本 次新修订《药品经营质量管理规范》(GSP)中,强化对于冷藏、冷冻药品温湿度控制要求,明确冷藏、冷冻药品在贮存、运输过程当中,必须配置相应的设施设 备,确保全过程冷链管理。同样,目的是降低由经营流通环节种由于经营企业温湿度控制工作执行不到位而造成冷链产品质变的风险,确保使用患者生命安全。
对比>>>
现行《药品经营质量管理规范》、2月20日修订草案、新修订后正式发布稿的变化
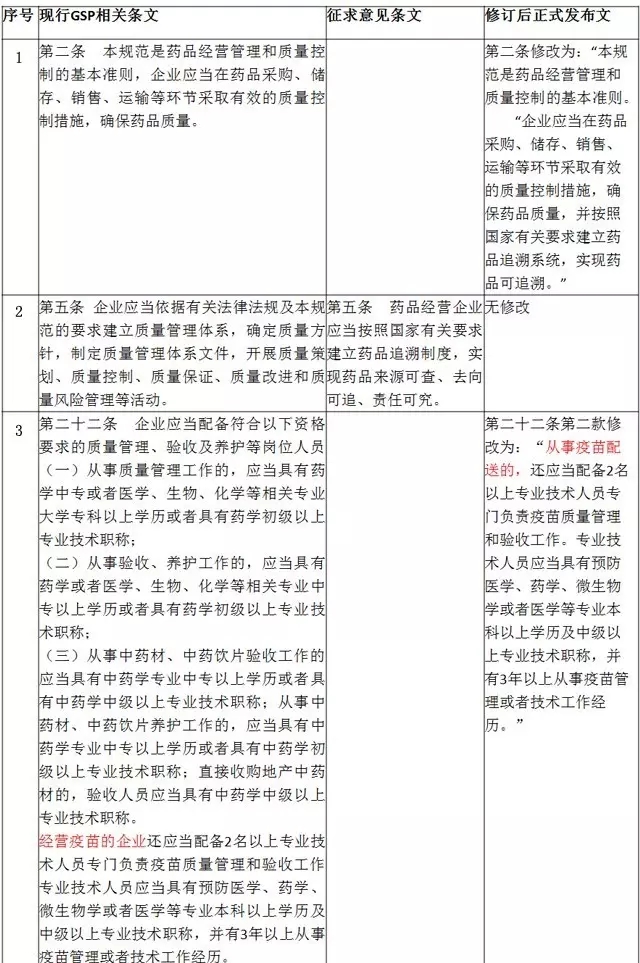

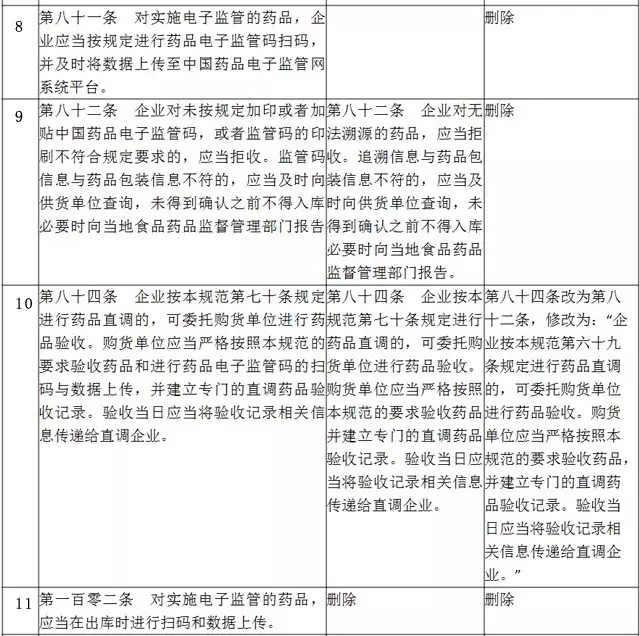

[/hide]
Tmall pharmacy stops to sell drugs online
On 29th July, Tmall pharmacy sent the notification to all online stores that the online drugs transactions will be stopped from 1st August. On 30th July Tmall pharmacy confirmed this news and said that according to the policy requirement from CFDA and Hebei Food and Drug Administration, the online drug retail business will be stopped. It is said that the reason for stopping the pilot Internet third-party platform of online drug retail is that some problems are exposed during the pilot process. For example, the responsibility of the third-party platform and the main body of the entity pharmacy is not clarified clearly; it is difficult to supervise the sale of prescribed drugs, and the safety and quality of drugs, which is not beneficial to protect the profit and drug safety of customers. (Source: Beijing Times)
天猫医药馆停止网上售药
来源:京华时报 2016-08-01
核心提示:7月29日,天猫医药馆向平台上商家发布通知,将于8月1日起停止药品在线交易功能。7月30日,天猫医药馆证实了此消息,并称此举是按照国家食药监总局和河北药监局的政策要求,停止药品网上零售业务。据报道称,互联网第三方平台药品网上零售试点结束的原因为“试点过程中暴露出第三方平台与实体药店主体责任不清晰、对销售处方药和药品质量安全难以有效监管等问题,不利于保护消费者利益和用药安全,因此决定结束互联网第三方平台药品网上零售试点工作。”
[hide for= “!logged”]
京华时报讯(记者苏季)7月29日,有报道称天猫医药馆向平台上商家发布通知,将于8月1日起停止药品在线交易功能。昨天,天猫医药馆向记者证实了此消息,并称此举是按照国家食药监总局和河北药监局的政策要求,停止第三方平台药品网上零售业务。
7月29日,有消息称天猫医药馆向平台上的商家发布了《2016年8月1日停止95095药品在线交易功能》的通知。通知称,“根据此前河北省食品药品监督管理局要求,我公司将于2016年8月1日停止药品在线交易功能,特此通知。”
此前一天,“互联网第三方平台药品网上零售试点工作结束”的消息出现在食药监总局的网站上。该局网站转载了中国医药(17.590, 0.00, 0.00%)报的一篇报道,该报道称,近日,食药监总局分别通知河北省、上海市、广东省食药监局,要求结束互联网第三方平台药品网上零售试点工作。
报道还提到了互联网第三方平台药品网上零售试点结束的原因,“试点过程中暴露出第三方平台与实体药店主体责任不清晰、对销售处方药和药品质量安全难以有效监管等问题,不利于保护消费者利益和用药安全,因此决定结束互联网第三方平台药品网上零售试点工作。”
食药监总局表示,结束第三方平台药品网上零售试点工作,不影响已经获取《互联网药品交易服务资格证书》的企业依照《互联网药品交易服务审批暂行规定》等规 定,继续开展企业对企业和医疗机构的药品交易服务业务;取得《互联网药品交易服务资格证书》的实体药店可以继续通过互联网直接向消费者销售药品。
2013年,食药监总局先后批准河北省、上海市、广东省的食药监部门在河北慧眼医药科技有限公司“95095”平台、广州八百方信息技术有限公司“八百方”平台和纽海电子商务(上海)有限公司“1号店”平台进行互联网第三方平台药品网上零售试点工作,试点期限为一年。
据了解,天猫医药馆2012年上线,此后阿里巴巴收购了95095医药平台。在此之前,天猫医药馆为拥有互联网药品交易服务资格证书(C类许可证)的药房提供技术支持和服务,帮助他们在线销售非处方药、医疗器械、隐形眼镜以及计生用品。
[/hide]
Shunfeng paticipates the distribution of second vaccination
For a long time, the distribution of second vaccination in China has been complex and complicated, so that the supply and service capacity of the industry is relatively bad. After the new policy about second vaccination in April 2016, the wholesale enterprises are out. The business of the logistics distribution is newly divided. On 28th June, the person in charge of cold transportation at Shunfeng said that the cold transportation at Shunfeng has already taken part in the distribution business of second vaccination. Shunfeng starts to deploy the cold-chain transportation capacity according to the situation of the whole industry. (Source: Caixin)
顺丰参与二类疫苗配送 规划布局冷链运输
来源:财新网 2016-07-05
核心提示:长期以来,中国二类疫苗流通环节错综复杂,也导致行业的供应及服务能力较差。今年4月,二类疫苗新政落地之后,批发企业出局,导致物流配送的蛋糕被重新划分。6月28日,顺丰医药冷运负责人马建聪表示,“顺丰冷运已经实际参与到二类疫苗的配送业务中,主要客户有例如辽宁成大生物股份有限公司、深圳赛诺菲巴斯德生物制品有限公司。”顺丰正针对整个行业的分布情况,开始配置冷链运输能力。
[hide for= “!logged”]
6月28日,顺丰医药冷运负责人马建聪表示,“顺丰冷运已经实际参与到二类疫苗的配送业务中,主要客户有例如辽宁成大生物股份有限公司、深圳赛诺菲巴斯德生物制品有限公司。”顺丰正针对整个行业的分布情况,开始配置冷链运输能力。今年4月,二类疫苗新政落地之后,批发企业出局,导致物流配送的蛋糕被重新划分。长期以来,中国二类疫苗流通环节错综复杂,整个医药冷链行业没有形成规模化、网络化的运输体系,也导致行业的供应及服务能力较差。
一位为外资疫苗生产企业提供省级经销服务的批发商透露,由于冷链环节投入高损耗大,且批发企业缺乏监管和追责压力,中途偷工减料现象非常普遍。“很多冷链车在长途运输中,中途都没有开制冷功能,临到卸货点再开制冷,检测温度也是合格的,但疫苗其实都报废了。”
医药冷链物流垄断现象显着。马建聪介绍说,冷链物流一般由药品商业流通主导,销售分销决定了冷链药品的流向,各个商业企业均根据自身的销售情况建立自 己冷链配送模式。相较而言,社会物流企业专业化程度低,缺乏冷链药品的配送经验和专业知识,如果没有进行专业的培训,在提供运输服务时容易发生运输风险, 从而导致药品企业不信任社会物流企业的冷链物流能力。另外,多级分销制导致冷链药品流通的环节多,各环节冷链物流能力参差不齐,运输过程质量难以管控。
4月25日,山东疫苗案之后,国务院颁布新政《国务院关于修改〈疫苗流通和预防接种管理条例〉的决定》(下称《决定》。新政规定,二类疫苗采购纳入省 级集中招标平台,二类疫苗批发企业全部出局,二类疫苗生产企业负责对接并配送到县级疾控机构,县级疾控机构再向下供应到各基层接种点。
医药冷链配送的难点在于经历多个物流环节,不同的环节使用不同的运输资源和信息系统,要实现药品流通全程的信息共享和全程温控,势必需要有统一的标准 和执行标准的能力。业内普遍认为,新政凸显了国家规范药品行业的决心,中国的医药冷链行业将在2016年进入高速发展的快车道。
“新政加强了行业监管的力度,规范了冷链运输标准,使药品生产企业、流通企业、物流企业开始正视药品冷链物流的质量。”马建聪表示,顺丰等专业物流公司具备丰富物流行业经验,能够从市场化的角度配置资源,进一步促进药品冷链物流行业快速发展。
在二类疫苗配送领域,疫苗生产商自建队伍、疾控系统自营冷链系统、疫苗批发企业转型、传统医药流通龙头及传统物流巨头将重新划分蛋糕。马建聪认为,冷 链药品物流未来的市场格局将分由两个部分做主力支撑:传统医药流通的巨头企业、社会物流企业中医药冷运的专业公司。“后者正在崛起中,物流服务的基因带给 这些企业以市场化和资源配置的不同角度,存在令药品流通行业的服务更加优质的竞争机会。”
但也有分析认为,顺丰等物流龙头企业花大价钱博取小市场并不划算,深度介入疫苗流通领域的可能性不大。安信证券研报认为,目前可能会接手疫苗配送业务 的有两种:国药等医药流通龙头冷链配送能力强,资源丰富,参与二类疫苗流通的概率较大;而疫苗厂商完全自营配送队伍的成本较高,有望与转型配送服务的原疫 苗批发企业再次携手合作。
顺丰则认为,作为具备丰富物流经验和运输管理能力的公司,顺丰拥有的网络覆盖资源不容小觑。“顺丰正在针对整个行业的分布情况,配置冷链运输能力,特 别是冷藏专用车辆。用于医药运输的专用冷藏车也分为干线运输车辆和支线运输车辆两种,其中干线车辆主要用于承接疫苗生产企业的整车运输业务,支线车辆主要 用于承接同省配送至区县疾控中心业务。从目前顺丰的业务布局看,支线车辆主要集中在四川、江苏、东北、广东等几个省份。”马建聪表示,顺丰作为民营企业在 投资管理模式和企业决策执行上具备更多活力,顺丰正在加大医药专用投资和人才配置,并发挥第三方平台的开放优势,在规范市场中获得发展机会。
[/hide]
The GSP certificates of seven pharmaceutical companies are withdrawn in Anhui
On 14th June, it was known from Anhui Food and Drug Administration that they had carried out flight inspection in the last one month, which has raised huge billows in the pharmaceutical industry nationally. The GSP certificates (Good Supply Practice for Pharmaceutical Products) of seven enterprises have been withdrawn in one month. (Source: Hefei Evening News)
安徽七家药企被收回GSP证书
来源:合肥晚报 2016-06-15
核心提示:昨日,记者从安徽食药监部门了解到,近一个月,安徽省食药监局开展飞行检查,频出重拳,在安徽甚至全国医药界掀起了巨大的波澜,一个月收回7家企业GSP证书,即《药品经营质量管理规范认证证书》。
[hide for= “!logged”]药品经营企业的GSP证书犹如司机的驾照,昨日,记者从安徽食药监部门了解到,近一个月,安徽省食药监频出重拳,在安徽甚至全国医药界掀起了巨大的波澜,一个月收回7家企业GSP证书,即《药品经营质量管理规范认证证书》。
安徽省食药监局开展飞行检查中发现,安徽省康元医药有限公司部分岗位、职责、权限管理混乱;冷库停用,库内无药品,温度显示为19.7℃,但检查发现公司仍有经营冷藏药品事实,如注射用头孢硫脒;大量的过期药品小儿化痰止咳颗粒存放在“合格区”。
在 安徽同安堂医药有限公司,发现票账货不符,在冷库内意外发现蛋肽类药品重组人促红素;中药材无专用库房和养护场所;阴凉库内内用药、外用药混垛。而安徽爱 特运通医药有限责任公司存在药品与非药品未分开储存、仓库药品储存较乱、温湿度监控数据记录不完整、发票管理较为混乱,部分药品销售未按相关要求开具发票 等问题。
安徽省柯斯达医药有限公司,存在仓库实际面积与《药品经营许可证》核准的实际面积不符:计算机系统库存与实际库存不符;未实施GSP定期内审;用于储存及运输低温药品的设施设备未经过验证;储运部岗位人员操作与授权范围不相符;阴凉库药品与非药品混放等问题。
在安徽天怡药业有限公司电脑系统里,查看的批次药品运输记录显示运输车辆车牌号与实际不符;无销售退回药品的验收记录;药品验收记录不全等。
在阜阳,检查发现安徽瑞泰药业有限公司存在中药饮片库、中药材库、药品库温湿度探头显示的温度,与用红外线测温仪测定的数据误差较大;冷库无温湿度数据记 录。而安徽阜阳润生源药业有限公司,则存在个别药品票账货不符;阴凉库内自动温湿度监测系统未及时校准,偏差较大;计算机岗位授权与其工作岗位职责不符; 未对购货单位提货人员身份进行核实等问题。
针对这些违法企业,安徽食药监局收回7家企业的GSP证书,并责令企业进行整改。
[/hide]
Tmall, 800Pharm and yhd.com announced the pause of the pharmaceutical businesses – all third party platforms of online drug selling pilots are called for a halt
Recently, Tmal Pharmacy, 800Pharm, and yhd.com announced the pause of the pharmaceutical businesses respectively. The third party platforms of online drug selling pilots are entirely called for a halt. These three pilots are at the moment the only platforms which got the pilot qualification of “Internet third party platforms of online drug selling”. Yhd.come announced that CFDA asks to stop the online drug selling pilots of third party platforms and that they got the announcement which was forwarded by Shanghai FDA. With respect to the reason of the pause, the officer from CFDA told the journalist from Caixin that there are problems of missing the supervision links for selling drugs online. CFDA are discussing about the solution. (Source: Sohu Health)
天猫医药馆、八百方、1号店分别宣布暂停药品业务 第三方平台药品网上零售试点被全面叫停
来源:搜狐健康 2016-06-06
核心提示:日前,天猫医药馆、八百方、1号店分别宣布暂停药品业务,第三方平台药品网上零售试点被全面叫停。这三家是目前唯一获得“互联网第三方平台药品网上零售”试点资格的三家平台。1号店在停止售药的说明中称:“1号店收到上海市食品药品监督管理局转达的通知,国家食品药品监督管理总局要求停止互联网第三方平台药品网上零售试点工作。”至于暂停的原因,国家食药总局人士接受财新记者采访时表示,网上售药面临监管环节缺失的问题,国家食药总局正在商讨解决方案。
[hide for= “!logged”]
日前,天猫医药馆、八百方、1号店分别宣布暂停药品业务,第三方平台药品网上零售试点被全面叫停。
缘何被叫停?
这三家是目前唯一获得“互联网第三方平台药品网上零售”试点资格的三家平台。公开资料显示,95095平台隶属于中信21世纪科技有限公司,其大股东是中信集团。八百方则是得到了广东省药监部门及南方医药经济研究所的指导,1号店则是源于1号店位居上海,得到位居改革前列、前卫开放的上海食药局的支持。
1号店在停止售药的说明中称:“1号店收到上海市食品药品监督管理局转达的通知,国家食品药品监督管理总局要求停止互联网第三方平台药品网上零售试点工作。”
这些第三方平台停止卖药似乎是国家局主动叫停,但是,据《北京青年报》的报道,国家食药监总局向北京青年报表示,目前总局没有发叫停通知,这是各省局的行为。
至于暂停的原因,国家食药总局人士接受财新记者采访时表示,网上售药面临监管环节缺失的问题,国家食药总局正在商讨解决方案。
医药电商受挫
互联网第三方平台药品网上零售试点被全部叫停后,意味着这些企业仅拥有《信息证》,对药品只能展示,不能销售,目前尚不能判断第三方平台今后能否再给持牌B2C网上药店引流。
对于不少B2C医药电商药企来说,天猫、1号店等既是展示的平台,其庞大点击量也是不少网上药店客流的重要来源。此次,这些医药电商公司虽然未受影响,但是,其平台本身客流量不大,所以,此次暂停销售对医药电商影响较大。上市公司太安堂在投资者互动平台上谈及天猫医药馆暂停药品销售对公司康爱多网上商城会有一定影响。
公开资料显示,天猫医药馆2012年正式上线,为拥有互联网药品交易服务资格证书(C类许可证)的药房提供技术支持和服务,同时向在线大药房商家收取最高为成交额3%的佣金。
天猫医药馆是阿里巴巴经营业务中增长最快的类目之一。2015财年,天猫医药馆的总商品交易额为47.4亿元人民币,占整个在线医药零售市场过半的份额。目前已有约258家大药房旗舰店入驻,而国内获得互联网药品交易B2C牌照的企业约为450家。
受流通行业大整治波及?
2014年5月,国家食药总局发布的《互联网食品药品经营监督管理办法(征求意见稿)》,明确开放处方药网上销售等政策,被认为医药电商一大政策。
两年多时间过去,网售处方药政策至今仍未有落地。有分析人士认为,这意味着医药电商遇冷。
分析人士对赛柏蓝表示,目前医药电商存在不少问题,个别网上药品经营者未取得互联网药品交易资质,非法从事药品销售;部分药品经营者通过网上非法发布药品信息,夸大宣传、夸大疗效;销售假药;个别合法网站违规售药,销售不该销售的药品,如处方药等问题。
但是,值得关注的是,这些问题大多出现在不具备医药电商资质的经营,具备医药电商资质企业一般合规经营。虽然如此,面对网上售药的问题,监管部门显得“有心无力”。目前,在国家对药品流通、销售渠道进行的大整治,作为药品销售渠道之一,如何加强对此渠道的监管也是国家局的重要挑战。
目前,国家局出台此政策,显示了国家局对药品流通全渠道加强监管和治理的决心,医药电商暂时也因此遇冷。
而从长远角度来讲,政策放开仍是大势所趋,八百方创始人张小兵曾在接受动脉网采访时表示:CFDA一直在积极推进医药电商行业的发展。
附:1号店说明全文
1号店关于互联网第三方平台医药网上零售试点停止的说明
2016年 6月 1日,1 号店收到上海市食品药品监督管理局转达的通知,国家食品药品监督管理总局要求停止互联网第三方平台药品网上零售试点工作。在接到该正式通知后,1号店立即 开展与第三方商家的沟通工作,最快在一周左右停止相关药品的销售,其他健康类的业务继续正常运营。
2014年 9月,1号店获得互联网第三方平台药品网上零售试点资格。近一年半的试点工作中,我们在各级食药监局的指导下落实试点政策,为广大顾客创造了安全可靠、便 捷快速的药品零售服务环境,也帮助企业搭建起了更直接有效的药品销售渠道,实现了在医药流通零售领域的有益探索。
对于此次的政策性调 整,1号店会严格按照国家食药监总局下达的要求,认真贯彻政策思想,仔细落实后续工作。与此同时,1号店将以顾客为先,随时关注政策的新进展,在合法合规 的前提下继续探索新型的业务模式,尽可能满足顾客所需,为顾客带来更优质的网购体验。
[/hide]

